Оголошення
Дослідницькі роботи і проєкти
Аналіз лікарських препаратів з вмістом органічних кислот
Учениця 9 класу у науково-дослідницькій роботі (проєкті) на тему "Аналіз лікарських препаратів з вмістом органічних кислот" знайомиться зі складом та методами аналізу лікарських засобів. Серед цих засобів визначають фізичні методи аналізу фармацевтичних препаратів та сировини, хімічні та біологічні методи аналізу.
Докладніше про роботу:
В навчальному дослідницькому проєкті з хімії учениця 9 класу самостійно здійснює аналіз лікарських препаратів, які вміщують органічні кислоти, а також в експериментальній частині роботи визначає реактиви та об’єкти дослідження, проводить якісний та кількісний аналіз спиртового розчину саліцилової кислоти.
Експериментально-дослідницька робота з аналізу лікарських препаратів з вмістом органічних кислот, що виконана ученицею 9 класу з хімії, містить експерименти з аналізу ацетилсаліцилової кислоти, зважування таблеток та визначення температури плавлення, а також дослід з перекристалізації ацетилсаліцилової кислоти.
Цей індивідуальний проєкт присв'ячений органічним кислотам, які містяться в лікарських препаратах. Тому учениця виконує цікаві дослідження з розчинності та кислотності ацетилсаліцилової кислоти, а також проводить якісний та кількісний аналіз ацетилсаліцилової кислоти. Проєкт відповідає на запит суспільства в високих вимогах до якості ліків та гарантуванні певного лікувального ефекту та безпечності їх дії на здоров’я людини.
Зміст
Вступ
1. Склад та методи аналізу лікарських засобів.
1.1 Склад лікарських засобів.
1.2 Фактори, що впливають на якість лікарського засобу.
1.3 Фізичні методи аналізу фармацевтичних препаратів та сировини.
1.4 Хімічні методи аналізу.
1.5 Біологічні методи аналізу.
Висновки до розділу.
2. Експериментальна частина.
2.1 Реактиви та об’єкти дослідження.
2.2 Якісний та кількісний аналіз спиртового розчину саліцилової кислоти.
2.3 Аналіз ацетилсаліцилової кислоти.
2.3.1 Зважування таблеток.
2.3.2 Визначення температури плавлення.
2.3.3 Перекристалізація ацетилсаліцилової кислоти.
2.3.4 Дослідження розчинності та кислотності ацетилсаліцилової кислоти.
2.3.5 Якісний та кількісний аналіз ацетилсаліцилової кислоти.
Висновки до розділу.
Висновки
Список використаних джерел
Додаток А
Вступ
Кількість лікарських засобів, що використовуються для лікування та профілактики різноманітних захворювань, із кожним роком збільшується. Для ефективного та безпечного їх застосування підвищуються вимоги до їх якості, що потребує розробку нових та удосконалення існуючих методів аналізу лікарських засобів.
Методи контролю якості лікарських засобів мають свої специфічні особливості, тому як лікарські препарати мають різну хімічну природу, різний стан (рідина, тверда речовина), до їх складу можуть входити декілька речовин, а деякі ліки є малостійкими при зберіганні. Аналізу піддаються не тільки ліки, а також сировина та речовини, що використовуються при виробництві лікарських засобів, проміжні сполуки при виробництві ліків, розчинники та допоміжні речовини, що входять до складу кінцевого продукту. Аналізу підлягає і готова фармацевтична продукція, тому як під час зберігання можуть змінюватися її властивості.
До аналізу лікарських засобів пред’являють високі вимоги, а процедура контролю якості та проведення аналізу відповідає законодавчим нормативам (та регламентується Державною Фармакопеєю України).
Для аналізу лікарських засобів використовують хімічні, фізичні, фізико-хімічні та біологічні методи, а також на попередньому етапі зовнішні спостереження (колір, запах, цільність, наявність осаду та ін.). Висновок про достовірність та якість лікарського засобу роблять на підставі результатів аналізу декількох проб.
Метою даної роботи було провести аналіз саліцилової кислоти (лікарська форма – спиртовий розчин саліцилової кислоти) і ацетилсаліцилової кислоти (лікарська форма – таблетка) за допомогою фізичних та хімічних методів та зробити висновок про достовірність та кількісний вміст основної речовини в досліджених фармацевтичних препаратів.
1. Склад та методи аналізу лікарських засобів
1.1. Склад лікарських засобів
До складу лікарського засобу входять основна сполука, що забезпечує певний лікувальний ефект та допоміжні речовини, що виконують різноманітні функції. Вміст допоміжних речовин не повинен перевищувати 20% маси лікарського засобу, при цьому повинні забезпечувати утворення однорідної легко дозованої маси, розчинення лікарської речовини з необхідною швидкістю, запобігання розпадання таблетки.
Допоміжні речовини, що входять до складу лікарських засобів виконують різноманітні функції: розріджують лікарську масу (крохмаль, буряковий цукор, молочний цукор, глюкозу, кальцію гідрофосфат, гідрокарбонат магнію, магнію окис, кальцію сульфат, натрію хлорид, магнію карбонат основний, сорбіт, сечовину та ін.); забезпечують розпадання таблетки в шлунку або в кишечнику при контакті з травними соками (желатин, агар-агар, метилцелюлоза, альгінова кислота; шипуча суміш гідрокарбонату натрію та лимонної кислоти; натрій лаурилсульфат, крохмаль та ін); забезпечують міцність капсул та таблеток, тобто склеюють складові таблетки ( глюкоза, етилцелюлоза, альгінова кислота, полівініловий спирт, біла глина, карбонат магнію, тальк та ін.). [1-3]
1.2. Фактори, що впливають на якість лікарського засобу
Основними джерелами забруднення лікарського засобу є апаратура, вихідна сировина, розчинники та інші речовини, які використовують при виготовленні препаратів. Дотримання технологічних вимог при виробництві (певної температури, тиску, кислотності, чистоти вихідних речовин) забезпечує отримання чистого продукту. Порушення всіх цих чинників може викликати побічні реакції, утворення продуктів розкладу та інших модифікацій продукту, що відрізняються фізико-хімічними властивостями та фізіологічною активністю. [1, 3].
При зберіганні лікарських засобів необхідно строго дотримуватися специфічних для даного лікарського засобу умов зберігання (температура, вологість, інтенсивність світла). Невідповідність умов зберігання також призводе до зміни складу та властивостей лікарського засобу.
1.3. Фізичні методи аналізу фармацевтичних препаратів та сировини
При аналізі лікарського засобу (або сировини) застосовують як інструментальні методи дослідження так і зовнішні спостереження. Простий зовнішній аналіз лікарського засобу дозволяє оцінити колір, запах, наявність осаду (у випадку рідких речовин), цілісність таблетки та упаковки та ін.
Після зовнішнього вигляду беруть серію проб лікарського засобу для аналізу відповідно до вимог Державної Фармакопеї України (ДФУ), яка містить загальні вимоги до лікарських засобів, та методики контролю якості лікарських засобів.
Фізичні методи ґрунтується на перевірці фізичних властивостей або вимірюванні фізичних характеристик препарату. Фізичні характеристики речовини часто виступають показниками його чистоти, завдяки чому їх визначення є необхідним етапом в процедурі аналізу фармацевтичних препаратів. До фізичних методів аналізу хімічної речовини відносять: агрегатний стан, визначення зовнішнього вигляду, забарвлення, щільності, вологості, температури плавлення, кипіння або затвердіння, показника заломлення, в’язкості та ін.
Температура плавлення речовини – це постійна величина, що наводиться у довідниковій літературі та характеризує дану речовину, її чистоту та справжність. Якщо речовина вміщує домішки, або під час зберігання препарату відбулися деякі хімічні процеси, температура плавлення даного продукту буде відрізнятися від температури плавлення чистої речовини.
Для деяких препаратів для визначення його чистоти використовують температуру затвердіння та температуру кипіння. Температура кипіння є характеристикою рідких речовини, значення температури повинно укладатися в певний інтервал, більш широкий інтервал свідчить про наявність домішок. Даний температурний показник для визначення чистоти продукти використовуються рідше, що обумовлено залежністю температури від атмосферного тиску та можливості утворення сумішей, що важко розділити.
Розчинність розглядається як орієнтовна характеристика лікарського засобу, за якою встановлюють його справжність і чистоту. [1]
1.4. Хімічні методи аналізу
До хімічних методів аналізу відносять якісні реакції на достовірність (хімічні реакції по визначенню катіонів, аніонів, функціональних груп), реакції визначення летючих сполук, вмісту води, вмісту кислот чи основ [1-3]. Для проведення якісного аналізу використовують реакції, що супроводжуються зміною кольору, випадом осаду. При проведенні аналізу використовують: а) загальні реакції, типові для цілого класу або групи сполук; б) специфічні реакції, типові для даної речовини, що дозволяють визначити її серед сполук даного класу, групи.
Показником ступеня чистоти лікарського засобу є визначення характеру середовища (кислотне або лужне). Водневий показник (рН) – це величина, що характеризує кислотність чи основність розчину (тобто надає інформацію про характер середовища) і дорівнює від’ємному значенню десяткового логарифма концентрації іонів Гідрогену рН = - lоg [Н+]. В залежності від водневого показника (змінюється в інтервалі 0 – 14) розрізняють: середовище нейтральне (рН=7), слабокислотне (рН = 3-7), слаболужне (рН = 7-11), сильно кислотне рН ‹ 3 та сильнолужне рН › 11.
Зміна (чи відхилення від заданого значення) характеру середовища є наслідком присутності домішок. Від значення кислотності середовища залежить термін зберігання лікарської сполуки та особливості її використання.
Кількісні методи хімічного аналізу дозволяють визначити у зразку кількісний вміст (концентрацію) окремих складових частин або домішок та кількісні співвідношення сполук, іонів і елементів, які входять до складу дослідних речовин. Кількісні методи хімічного аналізу підрозділяють на гравіметричний, титрометричний та кількісний елементний аналіз.
Гравіметричний (ваговий) базується на точному вимірюванні маси компоненту, що аналізується, в досліджуваному розчині. Титриметричний (об’ємний) визначає склад досліджуваної проби шляхом точного вимірювання об’єму розчину реагенту відомої концентрації (титранту), який взаємодіє в еквівалентних кількостях з речовиною, що визначається.
1.5. Біологічні методи аналізу
До біологічних методів дослідження відносяться випробування на токсичність, стерильність, мікробіологічну чистоту.
Проводять біологічні випробування на тваринах, окремих ізольованих органах, окремих групах кліток, певних штамах організмів. Активність препаратів виражають в одиницях дії. [3]
Висновки до розділу
Аналіз літературних даних свідчить, що лікарські засоби уявляють собою суміш сполук (основна сполука виявляє певний лікувальний ефект та допоміжні речовини, що виконують різноманітні функції). Якість сировини, що використовуються при виробництві ліків, дотримання технологічних вимог при виробництві впливають на якість готової продукції.
Для аналізу якості та достовірності лікарських засобів використовують фізичні, хімічні, біологічні методи дослідження та зовнішні спостереження.
За допомогою якісного хімічного аналізу доводять достовірність лікарського засобу. За допомогою кількісного аналізу визначають кількісний вміст складових частин і співвідносять результати з вимогами Державної Фармакопеї України.
2. Експериментальна частина
2.1. Реактиви та об’єкти дослідження
В роботі використовували: хлоридну кислоту (розбавлену та розчин з концентрацією 0.2 М та 0.1 М), розчин гідроксиду натрію (з концентрацією 0.5 М та 0.05 М), водний розчин ферум (ІІІ) хлорид (концентрація 0.001 М), дистильовану воду, оцтову кислоту (концентрація 1 М), фенолфталеїн (0.1 % розчин в 60% етиловому спирті).
В якості об’єктів дослідження було обрано саліцилову кислоту та ацетилсаліцилову кислоту (дані про виробника та концентрацію препарату наведено в табл. 2.1-2.2). Повний склад ацетилсаліцилової кислоти (допоміжні речовини та оболонка) наведено в Додатку А).
Таблиця 2.1. Саліцилова кислота (лікарська форма: розчин спиртовий нашкірний)
| № | Назва препарату | Виробник | Концентрація |
|---|---|---|---|
| 1 | Спиртовий розчин саліцилової кислоти | ТОВ «ДКП «Фармацевтична фабрика» (Житомирська область) | 1% (в 70% етиловому спирті) |
| 2 | -/- | ПАТ «ФІТОФАРМ» (Донецька область) | 1% (в 70% етиловому спирті) |
| 3 | -/- | ПАТ «Фармак» (м.Київ) | 2% (в 70% етиловому спирті) |
Таблиця 2.2. Ацетилсаліцилова кислота (лікарська форма: таблетки)
| № | Назва препарату | Виробник | Концентрація |
|---|---|---|---|
| 1 | Ацетилсаліцилова кислота | ПрАТ «Фармацевтична фірма «Дарниця» | 500 мг |
| 2 | Ацетилсаліцилова кислота | Корпорація "Артеріум" (м. Київ) |
500 мг |
| 3 | Ацетилсаліцилова кислота | Публічне акціонерне товариство «ЛУБНИФАРМ» | 500 мг |
| 4 | АСПИРИН® КАРДИО | Байер Биттерфельд ГмбХ, Німеччина | 100 мг |
2.2. Якісний та кількісний аналіз спиртового розчину саліцилової кислоти
В три окремі пробірки внесли по 2 мл кожного зразку досліджених препаратів. В кожну пробірку додали 1 мл водного розчину FeCl3, потім розділили отриманий в кожній пробірці розчин приблизно пополам. В 1-3 пробірки додали по 0.5 мл розведеної хлоридної кислоти, в 4-6 пробірки додали по 0.5 мл оцтової кислоти.
Зміни, що спостерігали під час проходження хімічних реакцій в пробірках для всіх досліджених зразків були однаковими. При додаванні розчину FeCl3 спостерігали фіолетове забарвлення розчину, при додаванні розбавленої хлоридної кислоти – знебарвлення розчину (а з часом спостерігали випадіння голчастих кристалів), при додаванні розчину оцтової кислоти – збереження фіолетового забарвлення розчину.
Перенесли 2 мл дослідженого розчину саліцилової кислоти в колбу, додали 3 краплі фенолфталеїну та додавали по краплям розчин основи (гідроксиду натрію) до появи стійкого малинового забарвлення. Експеримент повторили тричі для кожного зразка саліцилової кислоти. [4] Результати наведено в таблиці 2.3.
Таблиця 2.3. Результати кількісного аналізу препаратів саліцилової кислоти
| № | Об’єм NaOH, мл | Об’єм NaOH, мл | Об’єм NaOH, мл | Середнє значення | Процентний вміст саліцилової кислоти в препараті* |
|---|---|---|---|---|---|
| 1 | 2.75 | 2.8 | 2.8 | 2.78 | 0.97 % |
| 2 | 2.90 | 2.9 | 3.0 | 2.93 | 1.02 % |
| 3 | 5.80 | 5.85 | 5.85 | 5.83 | 2.01 % |
*Процентний вміст саліцилової кислоти в препараті розраховано за формулою 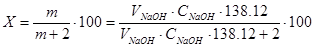 , де 138.12 – молекулярна маса саліцилової кислоти, 2 – об’єм розчину саліцилової кислоти, m – маса саліцилової кислоти.
, де 138.12 – молекулярна маса саліцилової кислоти, 2 – об’єм розчину саліцилової кислоти, m – маса саліцилової кислоти.
2.3. Аналіз ацетилсаліцилової кислоти
2.3.1. Зважування таблеток
За допомогою аналітичних терезів (ВЛА-200-М) визначили маси 3 таблеток кожної досліджуваної марки. Результати зважування наведено в табл. 2.4
Таблиця 2.4. Результати зважування таблеток ацетилсаліцилової кислоти
| Аспірин «Дариниця» | Аспірин «Артеріям» | Аспірин «Лубнифарм» | Аспірин Кардіо |
|---|---|---|---|
| 0.5920 / 0.5906 / 0.5913 г | 0.6494 / 0.6426 / 0.6542 г | 0.5749 / 0.5840 / 0.5745 г | 0.1327 / 0.1354 / 0.1350 г |
2.3.2. Визначення температури плавлення
Температуру плавлення визначали капілярним методом [5]. Таблетку подрібнювали до стану порошку. Потім порошок дослідженої речовини вносили до капіляру (довжина капіляру 40-50 мм, діаметр 1-1.5 мм, один кінець капіляру запаяний).
Досліджену речовину в капілярі струшували на запаяний кінець капіляру (декілька раз кидали капіляр в скляну трубку довжиною 75 см), доки стовпчик дослідженої речовини в капілярі досягне 3-4 мм. Далі капіляр укріплювали за допомогою резинового кільця до термометра (на рівні ртутної кульки). Прилад за допомогою якого визначали температуру плавлення наведено на рис. 2.1.
Нагрівання приладу проводили за допомогою газової горілки. Спочатку ( від 20 до 120 0С) нагрівали таким чином, щоб температуру підвищують на 5-8 оС за хвилину, а після 120 0С, зменшували нагрів, щоб температура піднімалася повільніше, приблизно 1-2 0С за хвилину. Початком плавлення є стан, коли речовина переходе в рідкий стан, а кінцем – утворення прозорої рідини.
Таблиця 2.5. Температура плавлення досліджених речовин
| 1 | 2 | 3 | 4 |
|---|---|---|---|
| 130 0C | 128 0C | 125 0C | 125 0C |
2.3.3. Перекристалізація ацетилсаліцилової кислоти
Роздрібнену до стану порошку наважку (0.04 г) ацетилсаліцилової кислоти переносили до фарфорової чашки та додавали 5 мл дистильованої води. Потім нагрівали до розчинення наважки. За допомогою шприцу затягували розчин, фільтруючи скрізь ватну пробку, потім охолоджували.
Осад, що випав відфільтровували на воронці з водоструминним насосом і сушили до постійної маси при 80-90 0С. Визначали температуру плавлення зразків 1 і 2 після перекристалізації згідно методики, що наведена в п.2.3.2. Результати наведено в табл. 2.6.
Таблиця 2.6. Температура плавлення досліджених речовин після перекристалізації
| 1 | 2 |
|---|---|
| 126 0C | 125 0C |
2.3.4. Дослідження розчинності та кислотності ацетилсаліцилової кислоти
Подрібнювали до порошкоподібного стану таблетки кожної марки. Наважку порошку ацетилсаліцилової кислоти (0.1 г) переносили до стакану та додавали 20 мл дистильованої води. Розділяли отриману суміш навпіл для кожної марки досліджуваних таблеток ацетилсаліцилової кислоти. Додавали до 1-4 пробірок по 1 мл розчину лугу (натрію гідроксиду з концентрацією 0.5 моль/л), рН розчину згідно універсального індикаторного паперу відповідало ~10.
В пробірки 5-8 додавали по 1 мл розчину кислоти (хлоридної кислоти з концентрацією 0.2 моль/л), рН розчину згідно універсального індикаторного паперу відповідало ~2. До наважки (0.1 г) кожного зразку ацетилсаліцилової кислоти додавали 10 мл етилового спирту. Зміни, що спостерігали в кожній пробірці наведено в табл. 2.7.
Таблиця 2.7. Розчинність ацетилсаліцилової кислоти у воді та етиловому спирті
| № | Розчинність у воді | Розчинність у воді при додаванні лугу | Розчинність у воді при додаванні кислоти | Розчинність в етиловому спирті |
|---|---|---|---|---|
| Частково розчиняється | Розчиняється | Частково розчиняється | Частково розчиняється (але більш ніж у воді) |
Наважку порошку ацетилсаліцилової кислоти (0.15 г) переносили до фарфорової чашки та додавали 15 мл дистильованої води. Витримували 5 хвилин та за допомогою універсального індикаторного паперу визначали кислотність середовища для кожної водної суспензії. Потім нагрівали кожну суспензію до кипіння (розчинення наважки) та знову визначали кислотність середовища за допомогою універсального індикаторного паперу. Результати спостережень наведено в табл. 2.8.
Таблиця 2.8. Результати дослідження кислотності
| № | рН до нагрівання | рН після нагрівання |
|---|---|---|
| 1 | 4 | 3 |
| 2 | 5 | 3 |
| 3 | 5 | 3 |
| 4 | 5 | 3 |
2.3.5. Якісний та кількісний аналіз ацетилсаліцилової кислоти
Наважку (0.25 г) досліджуваної речовини нагрівали з 4 мл розчину гідроксиду натрію до розчинення, потім додавали 5 капель сульфатної кислоти та спостерігали випадіння білого сніжистого осаду (що відповідає саліциловій кислоті). Осад відфільтровували, потім переносили до стакану і додавали 3-4 краплі розчину ферум (ІІІ) хлориду – спостерігали фіолетове забарвлення ( для всіх досліджених зразків).
Наважку препарату ( 0,5 г) розчиняли в 10 мл охолодженого до 8-10°С етиловому спирті. Додавали 3 краплі фенолфталеїну, потім додавали по краплям розчин основи (гідроксиду натрію) до появи стійкого малинового забарвлення. Зазначали об’єм основи, що витрачався на нейтралізацію кислоти. [4] Отримані дані наведено в табл. 2.9
Таблиця 2.9. Результати кількісного аналізу ацетилсаліцилової кислоти
| № | Вміст аспірину за результатами зважування* | Вміст аспірину за результатами титрування** |
|---|---|---|
| 1 | 84.45 %; 84.66 % | 83.39 %; 83.58 % |
| 2 | 76.98 %; 77.80 % | 84.34 %; 84.66% |
| 3 | 86.97 %; 85.73% | 84.55 %; 85.16% |
| 4 | 75.36 %; 74.07% | 86.34 %; 83.73 % |
Вміст аспірину за результатами зважування*: розраховували за формулою 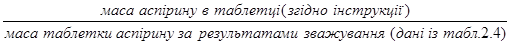
Вміст аспірину за результатами титрування**: розраховували за формулою [4] 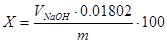 , де VNaOH – об’єм розчину основи, що пішов на титрування, мл; m – маса наважки препарату, що брали для аналізу, г; 0.01802 – кількість ацетилсаліцилової кислоти, що відповідає 1 мл 0.1 молярного розчина основи.
, де VNaOH – об’єм розчину основи, що пішов на титрування, мл; m – маса наважки препарату, що брали для аналізу, г; 0.01802 – кількість ацетилсаліцилової кислоти, що відповідає 1 мл 0.1 молярного розчина основи.
При роботі в хімічній лабораторії завжди використовувала халат, гумові рукавички, захисні окуляри. Всі роботи в лабораторії виконувалися під наглядом керівника.
Висновки до розділу
За допомогою якісної реакції з ферум (ІІІ) хлоридом доведена достовірність досліджених зразків саліцилової кислоти. Для всіх трьох зразків спостерігали: появу фіолетового забарвлення розчину, яке зникало при додаванні хлоридної кислоти.
Результати кількісного аналізу (методом титрування) свідчать, що вміст саліцилової кислоти 0.97% (ТОВ «ДКП «Фармацевтична фабрика»), 1.02% (ПАТ «ФІТОФАРМ») та 2.01% (ПАТ «Фармак»). Вміст кислоти в препараті повинен відповідати значенню від 0.95% до 1.05% або від 1.90% до 2.10%, тобто всі досліджені зразки цілком відповідають заявленої виробником концентрації.
Визначено температуру плавлення чотирьох зразків ацетилсаліцилової кислоти (виробництва ПрАТ «Фармацевтична фірма «Дарниця», Корпорація "Артеріум", ПАТ «ЛУБНИФАРМ», Байер Биттерфельд ГмбХ). Температура плавлення для всіх зразків відрізняється від табличного значення для чистої речовини, що пов’язано з вмістом допоміжних речовин в складі таблеток.
Всі досліджені зразки обмежено розчинні у воді, водному розчині кислоти та етиловому спирті, але розчинні у водному розчині лугу. Зразки ацетилсаліцилової кислоти виробництва Корпорації "Артеріум" та Байер Биттерфельд ГмбХ обмежено розчинні в воді при нагріванні.
Кислотність водного розчину з частково розчиненими таблетками ацетилсаліцилової кислоти у випадку «Аспірину» виробництва «Дарниця» найвища і відповідає рН 4, для зразків 2-4 відповідає рН 5, при нагріванні рН розчину становить для всіх водних сумішей 3.
За допомогою реакції з ферум (ІІІ) хлоридом доведена достовірність досліджених зразків аспірину (для всіх зразків спостерігали фіолетове забарвлення). Методом титрування визначено кількісний вміст ацетилсаліцилової кислоти в таблетках: 83.5%; 84%; 84.9%; 85%. Ці показники відповідають допустимій нормі вмісту основної сполуки в таблетках >80%. За результатами зважування та відповідності вмісту основної сполуки в препараті - менший вміст ацетилсаліцилової кислоти спостерігали для препаратів виробництва Корпорації "Артеріум" та Байер Биттерфельд ГмбХ, що вірогідно пов’язано з більшим вмістом допоміжних речовин у складі препарату.
Висновки
Досліджено лікарські препараті, до складу яких входять органічні кислоти: саліцилова кислота та ацетилсаліцилова кислота.
Проаналізовано три зразки спиртового розчину саліцилової кислоти (виробництва ТОВ «ДКП «Фармацевтична фабрика», ПАТ «ФІТОФАРМ», ПАТ «Фармак»). Доведена достовірність досліджених препаратів за допомогою якісної реакції з ферум (ІІІ) хлоридом.
За результати кількісного аналізу всі дослідженні зразки саліцилової кислоти цілком відповідають заявленої виробником концентрації.
Проаналізовано чотири зразки ацетилсаліцилової кислоти (виробництва ПрАТ «Фармацевтична фірма «Дарниця», Корпорація "Артеріум", ПАТ «ЛУБНИФАРМ», Байер Биттерфельд ГмбХ). Температура плавлення для всіх зразків відрізняється від табличного значення для чистої речовини, що пов’язано з вмістом допоміжних речовин в складі таблеток. Всі досліджені зразки «Аспірину» обмежено розчинні у воді, та в водному розчині кислоти, але розчинні в лужному розчині.
Кислотність водного розчину з частково розчиненими таблетками ацетилсаліцилової кислоти у випадку «Аспірину» виробництва «Дарниця» найвища і відповідає рН 4, при нагріванні рН водних сумішей ацетилсаліцилової кислоти всіх досліджених зразків становить 3. Достовірність досліджених препаратів доведена за допомогою якісної реакції (з ферум (ІІІ) хлоридом).
За результатами кількісного аналізу вміст ацетилсаліцилової кислоти в досліджених зразках відповідає допустимій нормі (> 80%).
Список використаних джерел
- Глущенко Н. Н. Фармацевтична хімія: Підручник для студ. середовищ. проф. навчань, закладів / Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков; Під ред. Т.В. Плетеневой. - Видавничий центр "Академія", 2004. - 384 с.
- Артеменко А.И. Застосування органічних сполук. - Дрохва, 2005. - 96 с.
- Машковский М.Д. Лікарські засоби: В 2 т. 13-е видавництво Харків: Торсинг, 1998. - Т. 1. - 506 с.
- Перельман Я.М. Аналіз лікарських засобів. Практичне керівництво, 1961.
- Техніка лабораторних робіт/ Ф.Ю. Рачинский, М.Ф. Рачинская : під ред. Д.П. Добычина Л. : Хімія, 1982. - 431
Додаток А
Ацетилсаліцилова Кислота-Дарниця
Виробник: ПрАТ «Фармацевтична фірма «Дарниця».
Склад лікарського засобу: 1 таблетка містить ацетилсаліцилової кислоти - 500 мг;
допоміжні речовини: кислота лимонна моногідрат, крохмаль картопляний.
Лікарська форма: таблетки.
Термін придатності 4 роки.
Умови зберігання: в оригінальній упаковці при температурі не вище 25 °С.
Ацетилсаліцилова кислота (acetylsalicylic аcid)
Виробник. Корпорація "Артеріум".
Склад лікарського засобу: 1 таблетка містить кислоту ацетилсаліцилову 500 мг;
допоміжні речовини: целюлоза мікрокристалічна (тип 102), крохмаль кукурудзяний, натрію кроскармелоза, аеросил магнію стеарату; оболонка: еудрагіт, метакрилатного сополімеру, полісорбат 80, натрію лаурилсульфат, триетилцитрат, тальк.
Лікарська форма: таблетки.
Термін придатності: 4 роки.
Умови зберігання: в сухому, захищеному від світла місці при температурі 15-25 ºС.
АЦЕТИЛСАЛІЦИЛОВА КИСЛОТА
Виробник: ПУБЛІЧНЕ АКЦІОНЕРНЕ ТОВАРИСТВО «ЛУБНИФАРМ»
Для медичного використання.
Склад лікарського засобу: 1 таблетка містить кислоти ацетилсаліцилової – 500 мг;
допоміжні речовини: крохмаль картопляний; тальк; кислота лимонна, моногідрат.
Лікарська форма: таблетки.
Термін придатності: 4 роки.
Умови зберігання: в оригінальній упаковці при температурі не вище 25 °С.
Аспирин® Кардио (Aspirin® Cardio)
Виробник: Байер Фарма АГ, 51368, Леверкузен, Німеччина.
Склад лікарського засобу: 1 таблетка містить кислоти ацетилсаліцилової 100 мг;
допоміжні речовини: порошок целюлози (10 мг), крохмаль кукурудзяний (10 мг),
оболонка: сопололімер метакрилової кислоти та етилкрилату 1:1(еудрагіт L30D,7.857 г); полісорбат 80 (0.186 мг), натрію лаурилсульфат (0.057 мг), тальк (8.1 мг), триетилцитрат (0.8 мг).
Лікарська форма: таблетка, вкрита оболонкою, що розчиняється в кишечнику.
Опис лікарської форми: круглі двояковипуклі таблетки білого кольору, з оболонкою білого кольору.
Термін придатності: 5 років
Умови зберігання: при температурі не вище 25 0С.
Нові проєкти і роботи
Навчальні програми
Банер сайту

Код банера: